Alkohol merupakan senyawa seperti air yang satu hidrogennya diganti oleh rantai atau cincin hidrokarbon. Alkohol mempunyai titik didih yang tinggi dibandingkan alkana-alkana yang jumlah atom C nya sama. Hal ini disebabkan antara molekul alkohol membentuk ikatan hidrogen. Rumus umum alkohol R – OH, dengan R adalah suatu alkil baik alifatis maupun siklik. Dalam alkohol, semakin banyak cabang semakin rendah titik didihnya. Sedangkan dalam air, metanol, etanol, propanol mudah larut dan hanya butanol yang sedikit larut. Alkohol dapat berupa cairan encer dan mudah bercampur dengan air dalam segala perbandingan.
Berdasarkan jenisnya, alkohol ditentukan oleh posisi atau letak gugus OH
pada rantai karbon utama. Ada tiga jenis alkohol antara lain
Penemaan senyawa alkohol dapat dilakukan dengan dua cara, yaitu berdasarkan aturan IUPAC dan cara Trivial.
Tata Nama Alkohol secara IUPAC.

Berdasarkan jenisnya, alkohol ditentukan oleh posisi atau letak gugus OH
pada rantai karbon utama. Ada tiga jenis alkohol antara lain
- Alkohol primer yaitu alkohol yang gugus –OH nya terletak pada C primer yang terikat langsung pada satu atom karbon yang lain contohnya : CH3CH2CH2OH (C3H7O).
- Alkohol sekunder yaitu alkohol yang gugus -OH nya terletak pada atom C sekunder yang terikat pada dua atom C yang lain.
- Alkohol tersier adalah alkohol yang gugus –OH nya terletak pada atom C tersier yang terikat langsung pada tiga atom C yang lain.
Tata Nama Alkohol
Penemaan senyawa alkohol dapat dilakukan dengan dua cara, yaitu berdasarkan aturan IUPAC dan cara Trivial.
Tata Nama Alkohol secara IUPAC.
1) Pemberian nama alkohol dilakukan dengan mengganti akhiran –a pada nama alkana dengan –ol. contoh :
2) Tentukan rantai utama (rantai dengan jumlah atom karbon paling panjang. Contoh:
3) Tentukan substituen yang terikat rantai utama. Contoh :
4) Penomoran substituen dimulai dari ujung yang terdapat gugus hidroksi (-OH) dengan nomor atom C paling rendah. Contoh :
5) Jika terdapat 2/lebih substituen berbeda, dalam penulisan harus disusun berdasarkan urutan abjad huruf pertama nama substituen. Contoh :
6) Awalan di-, tri-, sek-, ters-, tidak perlu diperhatikan dalam penentuan urutan abjad sedangkan awalan yang tidak dipisahkan dengan tanda hubung (antara lain : iso-, dan neo-) diperhatikan dalam penentuan urutan abjad. Contoh :
1) Tentukan gugus alkil yang mengikat gugus hidroksil. Contoh :
2) Tambahkan akhiran “alkohol” setelah nama substituen. contoh:
Perbandingan nama dengan sistem IUPAC dan Trivial.
| Rumus Molekul | Nama IUPAC | Nama Trivial |
| CH3-OH | Metanol | Metil Alkohol |
| C2H5-OH | Etanol | Etil Alkohol |
| C3H7-OH | Propanol | Propil Alkohol |
| C4H9-OH | Butanol | Butil Alkohol |
Sifat - Sifat Alkohol
Secara umum senyawa alkohol mempunyai beberapat sifat, sebagai berikut:
1) Mudah terbakar
2) Mudah bercampur dengan air semakin besar gugus alkil, maka kelarutan semakin kecil
3) Bentuk fasa pada suhu ruang :
– Alkohol dengan C 1 s/d 4 berupa gas atau cair
– Alkohol dengan C 5 s/d 9 berupa cairan kental seperti minyak
– Alkohol dengan C 10 atau lebih berupa zat padat
4) Pada umumnya alkohol mempunyai titik didih yang cukup tinggi dibandingkan
alkananya. Hal ini disebabkan adanya ikatan hidrogen atas molekulnya.
1) Mudah terbakar
2) Mudah bercampur dengan air semakin besar gugus alkil, maka kelarutan semakin kecil
3) Bentuk fasa pada suhu ruang :
– Alkohol dengan C 1 s/d 4 berupa gas atau cair
– Alkohol dengan C 5 s/d 9 berupa cairan kental seperti minyak
– Alkohol dengan C 10 atau lebih berupa zat padat
4) Pada umumnya alkohol mempunyai titik didih yang cukup tinggi dibandingkan
alkananya. Hal ini disebabkan adanya ikatan hidrogen atas molekulnya.
Reaksi Alkohol
1. Oksidasi
Alkohol dengan oksidator kuat seperti NA2Cr2O7 + H2SO4 dapat mengalami reaksi oksidasi. Hasil yang diperoleh dari reaksi oksidasi berbeda-beda tergantung pada jenis alkoholnya. Akohol primer jika teroksidasi menghasilkan aldehida apabila jumlah oksidator masih berlebih akan terjadi oksidasi berlanjut membentuk asam karboksilat, alkohol sekunder menghasilkan keton sedangkan alkohol tersier tidak bereaksi. Reaksi antara alkohol primer, sekunder dan tersier dengan K2Cr2O7 + H2SO4 dapat dilihat pada contoh.
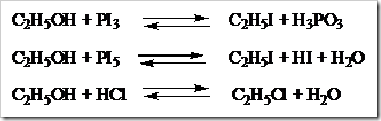
2. Penggantian Gugus –OH
Gugus –OH pada alkohol dapat digantikan oleh atom-atom halogen apabila direaksikan dengan fosfor halida dan asam halida. Fosfor halida dapat berupa PX3 dan PX5 sedangkan asam halogen berupa HX. Laju reaksi alkohol dengan asam halogen adalah alkohol tersier > alkohol sekunder > alkohol primer.
3. Dehidrasi alkohol
Apabila alkohol direaksikan dengan asam sulfat pada suhu 180 C maka akan terjadi reaksi dehidrasi dengan melepaskan air. Berikut reaksinya

4. Uji Lucas
- Pereaksi yang digunakan adalah ZnCl2 dan HCl
- HCl ditambahkan ke dalam sampel berisi ZnCl2 sehingga sistem mengalami kenaikan tingkat keasamaan
- Hasil akhir uji ini adalah suatu alkil klorida
- Pada alkohol tersier, reaksi berjalan lancar dan alkohol larut dalam air dan bereaksi dengan pereaksi Lucas membentuk alkil klorida yang sukar larut dalam air (mengingat alkil klorida adalah haloalkana bersifat nonpolar)
- Pada alkohol sekunder, reaksi berjalan sangat lambat sehingga dibutuhkan pemanasa sehingga terbentuk alkil klorida sukar larut dalam air
- Pada alkohol primer, pereaksi Lucas tidak akan bereaksi dengan alkohol dan terjadi endapan







Komentar
Posting Komentar